Como realizar las conversionesTemperatura °C, K y Presión Pa?
¿Por qué los alimentos se cuecen más rápido en una olla de presión?
En una olla normal con tapa, los alimentos reciben la presión atmosférica (1atm), y se logra una temperatura máxima de ebullición del agua, 100°C.
Para que el agua hierva a 100°C, el evento se realiza a nivel del mar (1 atm), si el experimento se llevara a cabo a una mayor altitud, tanto la presión atmosférica como el punto de ebullición disminuirían.
En una olla de presión, la presión que reciben los alimentos es mayor a la atmosférica (1 atm), a esta se agrega la presión por la acumulación de vapor de agua y el aumento en la temperatura de ebullición de 100°C. En un corto tiempo la presión total equivale a dos atmósferas (2 atm) y se mantiene constante debido a la válvula de seguridad que regula la salida de vapor cuando la presión sobrepasa cierto valor. Es por esto que se logra un cocimiento más rápido y por tanto un ahorro de energía.
La gráfica que relaciona la presión y la temperatura de una olla a presión no siempre es una recta, pero en la zona en que funciona normalmente podemos considerar que si lo es.
Al colocar un manómetro en una olla a presión, se obtuvo el siguiente resultado:
Temperatura (°C) Presión (Pa)
25 101,000
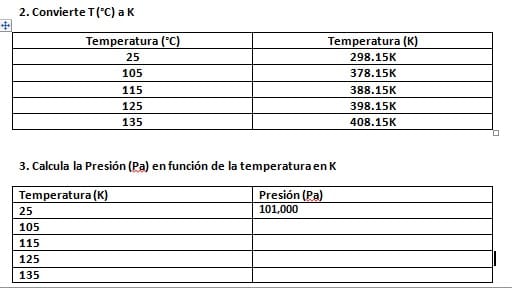
4. Grafica los datos de la tabla del inciso 3.
5. El funcionamiento de olla de presión es proporcional entre estos valores de presión y temperatura, como el volumen de la olla no cambia, ¿qué ley se puede aplicar para entender su comportamiento? Explica brevemente tu respuesta.
6. Organiza la información y resultados en un archivo, recuerda incorporar el problema, los resultados de las tablas (incisos 2 y 3) con su procedimiento y solución; la gráfica con los resultados obtenidos, así como la pregunta y respuesta del punto 5.
